开发能够在外源信号控制下精准遥控活体化学反应的技术,对于揭示复杂生物过程机制及发展精准治疗策略具有重要价值。然而,构建在体内按需激活的分子体系仍面临双重挑战:既需要具备优异生物相容性的化学反应以调控分子功能,又需要能够有效穿透组织且安全的触发方式。近年来,基于光或辐射等物理刺激的远程激活策略虽然取得了进展,但光控反应受限于组织穿透深度,而辐射则面临生物安全性、设备成本及操作复杂性等问题。相比之下,超声波具有组织穿透力强、生物安全性高且设备普及等显著优势,是极具潜力的活体内分子激活手段。此前研究者已探索了基于超声响应的载体释放、化学键断裂或化学转化等策略,但开发简便、普适的声控激活反应仍是该领域的重点。
近日,陈鹏和樊新元课题组在Angewandte Chemie International Edition上发表了题为 “Remote Molecule Activation in Living Mice Triggered by Therapeutic Ultrasound” 的研究论文。该研究报道了一种由治疗性超声触发的脱硼羟基化反应(Deboronative Hydroxylation triggered by Ultrasound,简称 dBus),实现了对荧光分子、小分子药物及生物大分子在活体环境下的声控激活(图 1)。
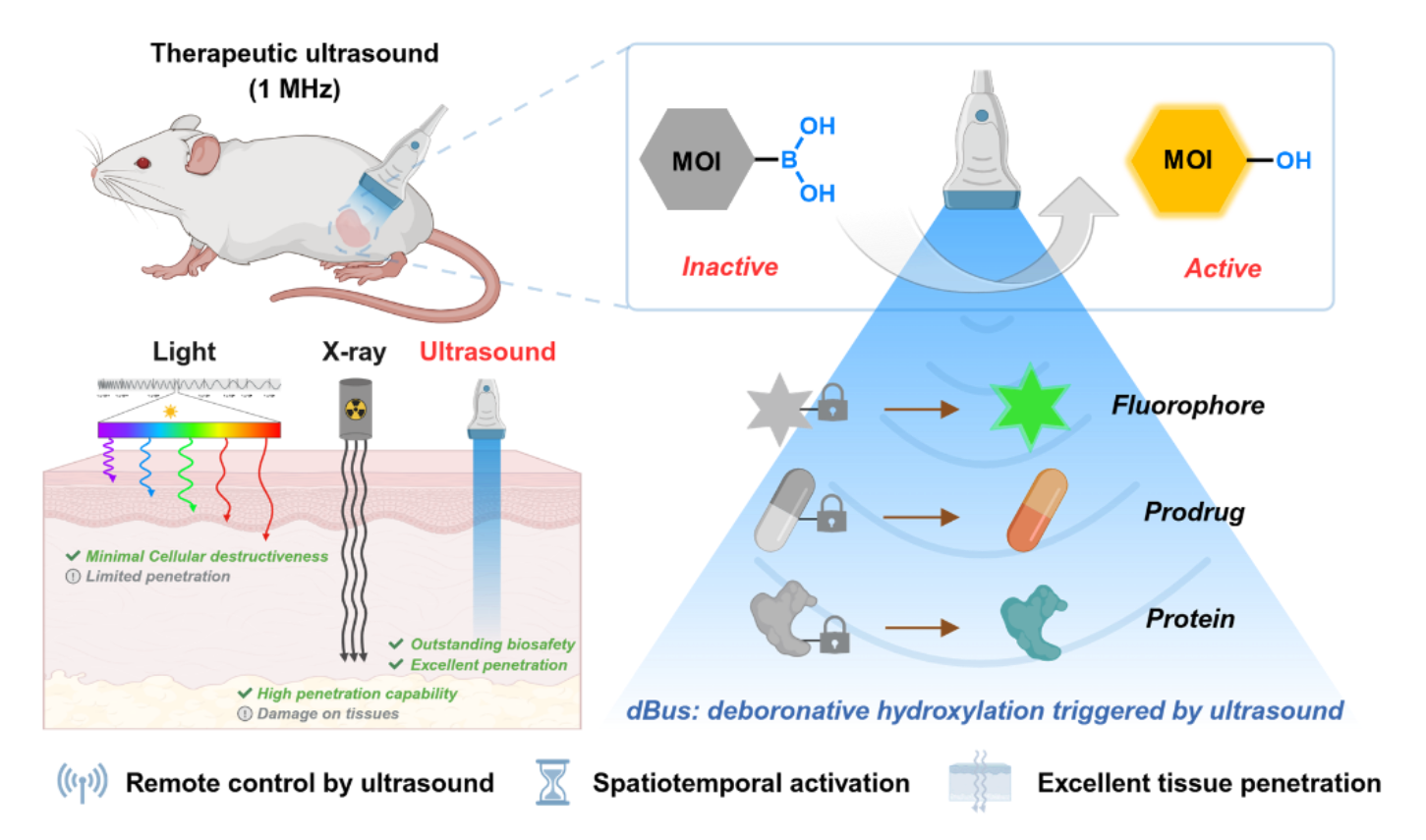
图1 超声触发脱硼羟基化反应(dBus)
在 dBus 技术的开发过程中,作者发现苯基硼酸类化合物在治疗性超声作用下可选择性转化为酚类衍生物 。以硼酸基团保护的荧光探针 Fluo-BA 为模型,实验证实超声处理可诱导荧光信号逐渐增强,成功实现分子激活 。机理研究揭示,治疗性超声通过声空化效应在水相介质中产生羟基自由基(•OH),这是驱动脱硼羟基化转化的关键活性物种 。电子顺磁共振(EPR)实验捕捉到了 BMPO-OH 加合物特征性的 1:2:2:1 四重峰信号,为 •OH 的生成进一步提供了证据(图2)。
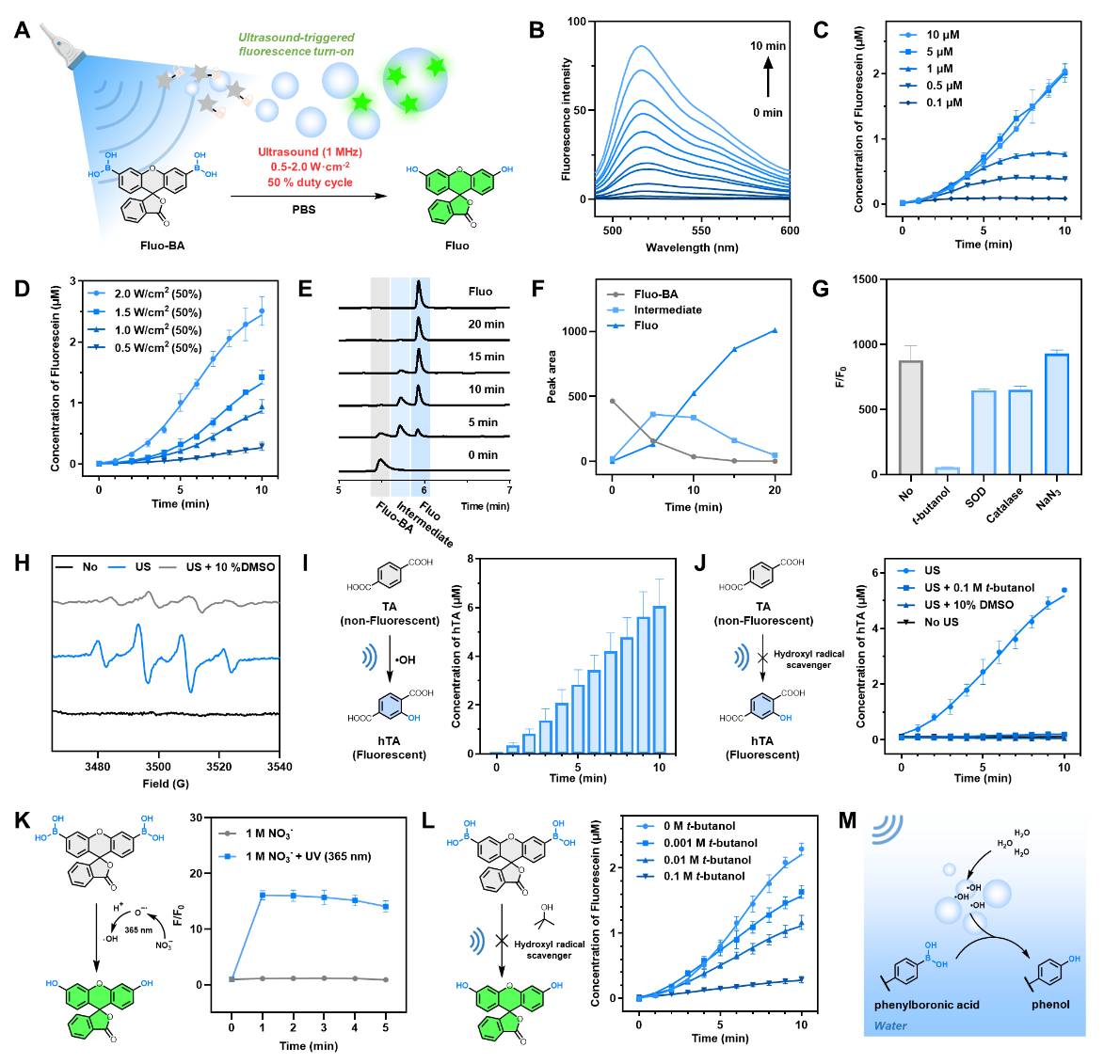
图2 dBus的发现与机理研究
基于上述机理,作者在多种功能分子骨架中策略性引入硼酸基团,构建了声控激活体系(图 3)。在小分子药物层面,作者合成了抗肿瘤药物阿霉素(Dox)和 SN38 的前药衍生物 Dox-BA 与 SN38-BA 。实验显示,这些前药在常规条件下保持惰性,仅在超声处理后释放活性药物,对肿瘤细胞表现出显著的杀伤效果 。此外,dBus 技术还成功应用于共价标记探针 QM-Bio-BA 的激活,实现了对蛋白质的高效生物素化标记。dBus 技术的普适性进一步拓展至生物大分子领域。作者证明该反应可用于多肽侧链保护基的脱除,成功实现了 NYESO 肽和抗癌肽 MMAE 的原位释放 。在蛋白质层面,通过遗传密码扩展技术,作者构建了定点包含硼酸保护型酪氨酸(Tyr-BA)的 GFP 突变体。质谱分析显示,超声处理后蛋白质分子量发生 28 Da 的特征性减小,证实了蛋白侧链在分子层面的精准转化。
最后,作者评估了 dBus 在活体系统中的转化潜力。组织穿透实验证实,治疗性超声可有效穿透厚度达 3 厘米的生物组织并触发化学反应 。在肿瘤移植瘤模型中,Dox-BA 与超声联合处理组显示出显著的肿瘤生长抑制效果,其疗效与直接使用 Dox 相当 。关键优势在于安全性,Dox 处理组小鼠出现严重体重下降和肝肾生化指标异常,而 dBus 组小鼠体重保持稳定且各项生化指标正常,实现了“外源可控且减毒增效”的治疗目标 (图3)。
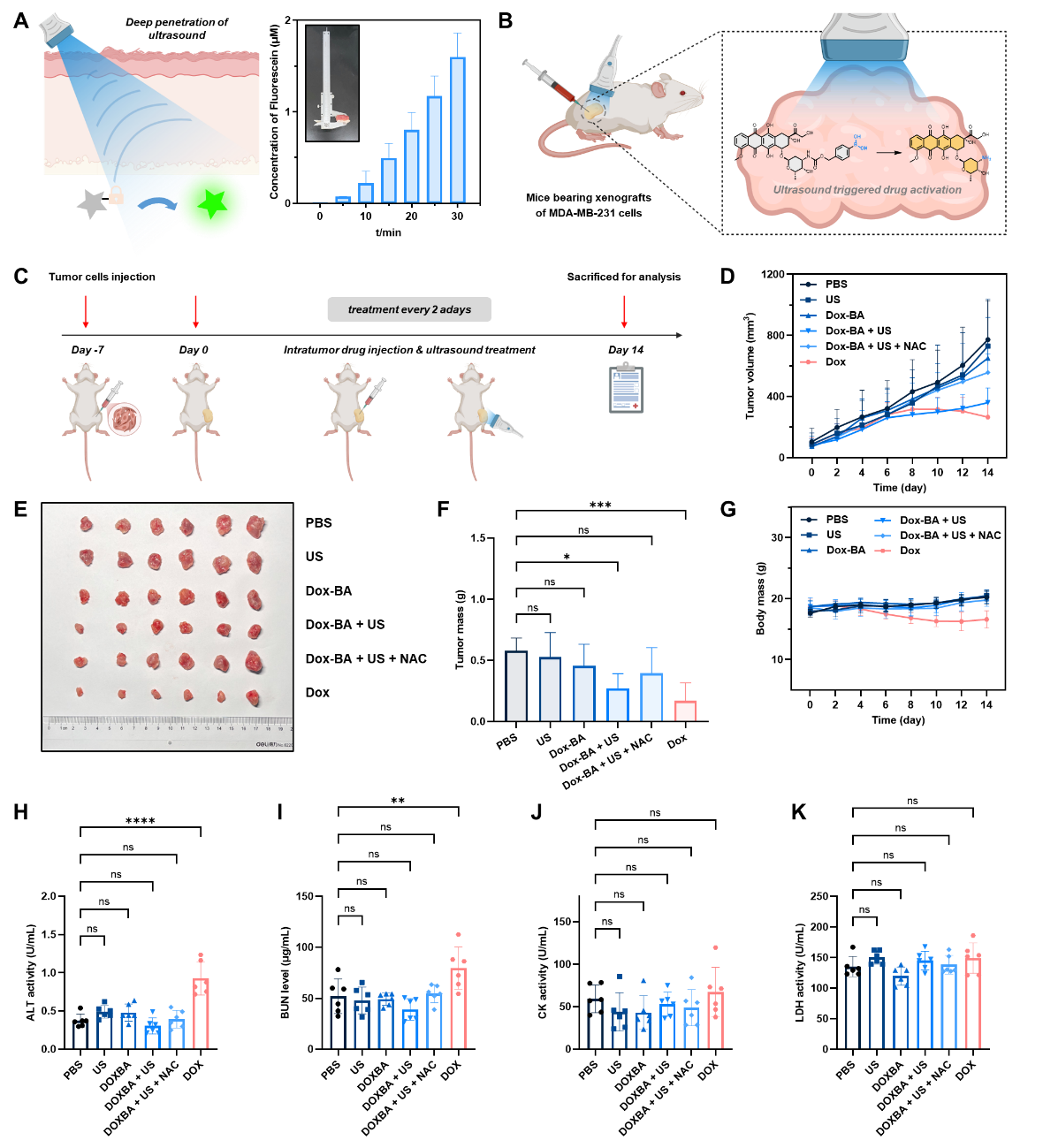
图3 dBus反应实现活体小鼠中外源可控的声控药物激活
总结而言,该研究开发了一种通用的超声触发化学平台 dBus。该技术利用临床兼容的治疗性超声参数(1 MHz, 0.5 – 0.75 W/cm2),通过精准控制自由基化学反应,克服了传统光控或放射激活策略的局限性。dBus 凭借其优异的组织穿透性、生物相容性和模块化设计,为声药理学及深层组织生物医学干预提供了坚实的化学基础。
北京大学化学与分子工程学院樊新元和陈鹏教授为该文的通讯作者,博士研究生覃圣男为该论文的第一作者。该研究工作得到了国家重点研发计划、国家自然科学基金及北京市自然科学基金等项目的资助与支持。
原文链接:
Remote Molecule Activation in Living Mice Triggered by Therapeutic Ultrasound
Shengnan Qin, Xuan Liang, Yufei Di, Ziqi Liu, Zhizheng Lou, Xinyue Chen, Peng R Chen*, Xinyuan Fan*
https://doi.org/10.1002/anie.202525894
排版:高杨
审核:牛林,刘志博